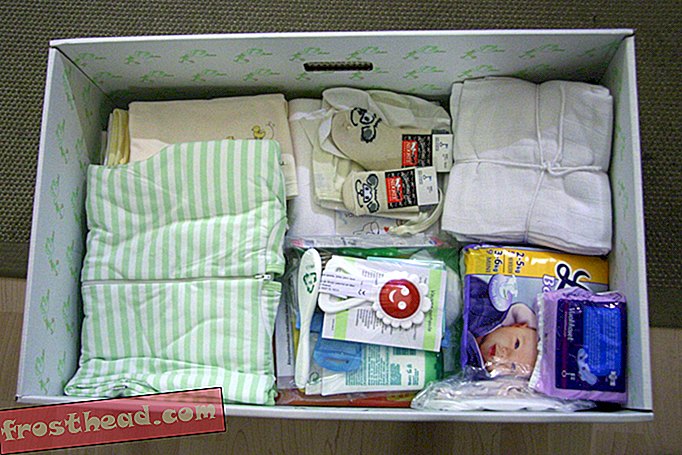
1960. godine Amerika je imala sreću. Tada je aplikacija za početak masovnog stavljanja u promet lijeka talidomida u Sjedinjenim Državama sletila na stol Frances Oldham Kelsey, recenzenta u Upravi za hranu i lijekove. Danas znamo da lijek može uzrokovati niz teških urođenih deformiteta, pa čak i smrt dojenčadi kada ih trudnice uzimaju zbog mučnine. Ali u to su vrijeme tamni učinci talidomida tek postali poznati.
Povezani sadržaj
- Upoznajte računalnog znanstvenika kojem biste trebali zahvaliti na vremenskoj aplikaciji vašeg pametnog telefona
- Proizvođač talidomida na kraju se ispričava zbog urođenih mana, preživjeli kažu da to nije dovoljno
Između 1957 i 1962, sedativ bi rezultirao tisućama dojenčadi u Kanadi, Velikoj Britaniji i Zapadnoj Njemačkoj rođenih s ozbiljnim deformitetima, uključujući skraćivanje ili odsutnost udova. SAD, međutim, nikada nisu imale krizu taformomida povezanih talidomida te veličine. Zašto ne?
Ono što je stajalo između droge i zdravlja američke javnosti nije bilo ništa drugo do Kelsey i FDA. Kao liječnički pregled, Kelsey je imao moć spriječiti izlazak lijeka na tržište ako utvrdi da aplikacija nema dovoljno dokaza za sigurnost. Nakon temeljitog pregleda Kelsey je odbio zahtjev za talidomidom iz razloga što nedostaje dovoljno dokaza sigurnosti kroz rigorozna klinička ispitivanja.
Danas smatramo zdravo za gotovo da je FDA mudro potaknuo nesigurni lijek. Ali na mnogo načina, Kelseyjevo obrazovanje i iskustvo do tog trenutka učinili su je posebno prikladnom za položaj liječničkog pregleda -, a posebno za primjenu talidomida.
Nakon završetka magistarskog studija farmakologije na sveučilištu McGill u svojoj domovini Kanadi, diplomirani savjetnik Kelsey preporučio je dr. Eugeneu Geilingu na Sveučilištu u Chicagu da se raspita o položaju asistenta i izrazio zainteresiranost za stjecanje doktorata. Geiling, medicinski službenik FDA-e poznat po svojim studijama hipofize, uzvratio je nudeći Kelseyu pomoć u istraživanju i stipendiju za doktorski studij. 1936. Kelsey se pridružio Geilingu na University of Chicago.
Taj posljednji korak u Kelseyjevoj karijeri možda je posljedica slučajne pogreške Geilinga. U svom kratkom memoaru "Autobiografske refleksije", Kelsey opisuje Geilinga kao "vrlo konzervativnog i staromodnog", napominjući kako se "zaista nije previše držao prema ženama kao znanstvenicima." To bi moglo objasniti zašto Geiling, u svom odgovoru Kelseyju, obratio ga „Mr. Oldham ”- vjerujući joj da je muškarac. Kelsey je rekla da se i dalje pita „da li sam se zvala Elizabeth ili Mary Jane, bih li postigla taj prvi veliki korak.“
Kelsey je prvi put upoznat s opasnostima masovno plasiranih nesigurnih lijekova 1937. godine, kada je FDA registrirala Geilinga kako bi riješila misteriju eliksira sulfanilamida. Sulfanilamid se učinkovito borio s infekcijama, ali našao se u velikoj i gorkoj tableti koju je trebalo uzimati u velikim dozama. Kako bi lijek bio što privlačniji, posebno djeci, proizvođači su ga dodali u otapalo s umjetnom aromom maline.
Problem je bio što je otapalo koje su odabrali bio dietilen glikol - obično poznato kao antifriz. Između rujna i listopada droga je ubila 107 osoba.
Geiling i njegov laboratorij studenata, uključujući Kelseyja, namjeravali su odrediti što točno u eliksiru ubija ljude: otapalo, aroma ili sulfanilamid. Kroz niz studija na životinjama - koje u to vrijeme savezni zakon nije zahtijevao da bi lijek mogao ići na tržište - Geiling i njegov laboratorij mogli su utvrditi da je dietilenglikol uzrok smrti.
Javno negodovanje zbog ove tragedije potaknulo je Kongres da donese Savezni zakon o hrani, lijekovima i kozmetici iz 1938., kojim je dodan novi odjeljak o lijekovima koji zahtijeva da proizvođači predoče dokaze da je lijek siguran prije nego što izađe na tržište. Iako je ovaj novi zakon „predvidio distribuciju novog lijeka u svrhu testiranja“, povjesničar FDA-e John Swann kaže „zakon nije na jasan ili detaljan način predvidio način provođenja nadzora nad tim testiranjem.“ Drugim riječima, klinička ispitivanja i dalje podvrgnut malo nikakvom nadzoru.
 1962. predsjednik John F. Kennedy odlikovao je Kelseyja zbog njezinog rada blokirajući tržište talidomida. (Uprava za hranu i lijekove)
1962. predsjednik John F. Kennedy odlikovao je Kelseyja zbog njezinog rada blokirajući tržište talidomida. (Uprava za hranu i lijekove) Kelsey je diplomirala medicinsku školu 1950. godine i nastavila raditi u časopisu Američkog medicinskog udruženja prije nego što je 1960. godine započela rad kao medicinska recenzentica pri FDA. Kao recenzentica novih aplikacija za lijekove (NDA) bila je jedna od tri osobe na teret određivanja sigurnosti droge prije nego što je mogao biti dostupan za javnu potrošnju. Kemičari su pregledali kemijsku sastav lijeka i kako proizvođač može jamčiti njegovu konzistenciju, dok su farmakolozi pregledali ispitivanja na životinjama koja su pokazala da je lijek siguran.
Iako se čini da je to strog i temeljit postupak provjera i ravnoteže, Kelsey je priznala neke slabosti u svom memoaru, uključujući i činjenicu da su mnogi medicinski pregledavači bili honorarno, premalo plaćeni i simpatični prema farmaceutskoj industriji. Najviše zabrinjavajući nedostatak u procesu bio je 60-dnevni prozor za odobravanje ili odbijanje lijekova: Ako prođe 60. dan, lijek bi automatski krenuo na tržište. Podsjeća da se to dogodilo barem jednom.
Srećom, NDA za Kevadon - proizvođač lijekova Richardson-Merrell - američki trgovački naziv za talidomid - bila je tek druga primljena NDA Kelsey, što znači da još uvijek nije imala zaostatke u pregledima. Za Kelseyja i ostale recenzente, talidomid nije prošao skupinu. Ne samo da je bilo farmakoloških problema, nego je Kelsey smatrao da su klinička ispitivanja nevjerojatno nedovoljna jer su izvješća liječnika bila premala i da su se uglavnom temeljila na svjedočanstvima liječnika, a ne na dobroj znanstvenoj studiji. Odbila je prijavu.
Izvješća o perifernom neuritisu s nuspojavama - bolnoj upali perifernih živaca - objavljena su u broju za britanski medicinski časopis u prosincu 1960. godine. Ovo je podiglo još veću crvenu zastavu za Kelseyja: "periferni neuritis nije bio vrsta nuspojave koja bi trebala poticati od obične tablete za spavanje."
Zatražila je više informacija od Merrell-a, koji je odgovorio drugom aplikacijom samo navodeći da je talidomid barem sigurniji od barbiturata. Zatim je Kelsey direktno poslala pismo Merrellu u kojem je navela da sumnja da znaju za neurološku toksičnost koja je dovela do upale živaca, ali odlučila je ne otkriti u svojoj prijavi. Merrell se sve više uzrujavala što Kelsey neće prenijeti njihov lijek koji je u ovom trenutku bio korišten u preko 40 drugih zemalja.
Ako se neurološka toksičnost razvila kod odraslih koji su uzimali talidomid, Kelsey se pitao: Što se događa s fetusom trudnice koja je uzimala lijek? Njezina zabrinutost pogodila je koji bi bio najopasniji učinak talidomida u drugim zemljama.
Kelsey je ranije postavljao ta pitanja. Nakon što je doktorirala. 1938. ostala je kod Geilinga. Tijekom Drugog svjetskog rata, Geilingov se laboratorij pridružio širokom pokušaju pronalaženja liječenja od malarije za vojnike u ratnim vremenima. Kelsey je radio na metabolizmu lijekova u kunića, posebno enzima u jetri koji im je omogućio da lako razgrade kinin. Ono što nije bilo jasno jest kako je ovaj enzim razgradio kinin u trudnih zečeva i u zečjim embrionima.
Kelsey je otkrio da trudni kunići ne mogu tako lako razgraditi kinin i da ga embriji uopće ne mogu razgraditi. Iako je već učinjeno na učinku lijekova na embrione, ono još nije bilo dobro istraženo područje.
Do studenog 1961., liječnici u Njemačkoj i Australiji neovisno su otkrili urođene mane u novorođenčadi čije su majke uzimale talidomid tijekom rane trudnoće. U embrija, talidomid može uzrokovati kritičnu štetu u razvoju organa - čak samo jedna pilula može rezultirati deformacijama novorođenčadi. A s obzirom da su mnogi liječnici propisali talidomid za liječenje jutarnje mučnine bez recepta, oboljelo je 10 000 novorođenčadi širom svijeta, a bezbroj drugih umrlo je utero.
Merrell je na kraju povukao prijavu samostalno u travnju 1962. Međutim, lijek je već bio distribuiran "više od 1200 liječnika, oko 15.000-20.000 pacijenata - od kojih je preko 600 trudnica", prema Swan-u. U SAD-u je prijavljeno 17 slučajeva urođenih deformiteta, ali kako Swan kaže putem e-pošte, „to bi moglo biti na hiljade da FDA nije inzistirala na dokazima sigurnosti potrebnim prema zakonu (unatoč stalnom pritisku sponzora droge)“.
1962., ubrzo nakon što je Merrell povukao njihovu primjenu i opasnosti od droge postale međunarodno poznate, Kongres je usvojio amandman Kefauver-Harris. Ova ključna izmjena zahtijevala je veći nadzor kliničkih studija, uključujući informirani pristanak pacijenata u studijama i znanstvene dokaze o učinkovitosti lijeka, a ne samo njegovu sigurnost. Nakon prolaska, predsjednik Kennedy dodijelio je Kelseyu predsjedničku nagradu za istaknutu saveznu civilnu službu, čime je postala druga žena koja je dobila tako visoku civilnu čast.
U svom memoaru Kelsey kaže da čast nije pripala samo njoj. "Mislila sam da medalju prihvaćam u ime mnogih različitih federalnih radnika", piše ona. "Ovo je zaista bio timski napor." 1963. brzo je promaknuta u šefa istražnog ogranka droge, a četiri godine kasnije postala je direktorica Ureda za znanstveno istraživanje - mjesto koje je obavljala 40 godina dok se nije umirovila u u dobi od 90. Živjela je do 101. godine života, a preminula je 2015. godine.
Kelsey je provela većinu svog života u javnoj službi, a njezina se priča i dalje ističe kao svjedočanstvo o bitnoj ulozi FDA-e u održavanju sigurnosti droga.
Napomena urednika, 14. ožujka 2018. godine: Ovaj je članak ažuriran kako bi odražavao točan i prikladan jezik prema stilskom vodiču Nacionalnog centra za osobe s invaliditetom.